Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Подготовка к ЕГЭ по химии 11 класс
Содержание
- 1. Подготовка к ЕГЭ по химии 11 класс
- 2. Цели:Ознакомиться с материалом экзаменационной работы по химии.Проверить
- 3. В презентации представлены задания из
- 4. Неверно НеверноНеверноВерно 1) верны оба суждения2) обы
- 5. Верно НеверноНеверноНеверно 4) 8,4 г2) 4,2 г1)
- 6. Верно НеверноНеверноНеверно 4) 5,6 л2) 22,4 л1)
- 7. Неверно НеверноНеверноВерно 1) 502) 404) 60 3)
- 8. B1. Установите соответствие между названием вещества и
- 9. B2. Установите соответствие между названием вещества и
- 10. B3. Установите соответствие между веществом и продуктом
- 11. B4. Установите соответствие между формулой соли и
- 12. B5. Установите соответствие между реагентом и продуктом
- 13. B6. Установите соответствие между двумя веществами
- 14. НеверноВерноНеверноНеверно4) 1351) 2362) 1343) 145 B7. Как
- 15. НеверноВерноНеверноНеверно4) 4561) 2352) 1563) 146 B8. Метанол вступает в реакции сCH3COOHNaOHAg2O(NH3)Br2(H2O)KMnO4(H+)Na
- 16. НеверноВерноНеверноНеверно4) 2341) 1362) 2563) 145 B9. И
- 17. C1. Используя метод электронного баланса, составьте уравнение
- 18. C2. Медь растворили в концентрированной серной кислоте.
- 19. C3. Напишите уравнения реакций, с помощью которых
- 20. C4. Сероводород, выделившийся при взаимодействии избытка концентрированной
- 21. C5. При взаимодействии 11,6 г предельного альдегида
- 22. Слайд 22
- 23. х
- 24. Литература:1. Открытый банк заданий ЕГЭ http://www.fipi.ru/os11/xmodules/qprint/afrms.php?proj=2. http://chem.reshuege.ru/test?theme=203.
- 25. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1
Подготовка к ЕГЭ по химии
Работу выполнила учащаяся 11 «а» класса
МБОУ СОШ №26 Козина Лариса.
Слайд 2Цели:
Ознакомиться с материалом экзаменационной работы по химии.
Проверить свою подготовленность к
экзамену.
Расширить опыт выполнения тестовых заданий по химии
Слайд 3 В презентации представлены задания из трех частей:
часть
«А» в виде тестов – 28 заданий с одним правильным
ответом;часть «В» – 9 заданий (В1-6 - с выбором 4 цифр – цифры могут повторяться, В7-9- с выбором трех последовательных цифр
часть «С» – 5 заданий с развернутым ответом.
Чтобы выбрать правильный ответ на вопрос части А1-28 наведите курсор на выбираемый ответ и кликните на левую кнопку мышки, при правильном ответе появится слово «Верно», при неправильном - «Неверно»
Ответы и решения заданий части С1 – С5 появятся по щелчку
Инструкции и рекомендации:
ТР
ТМ
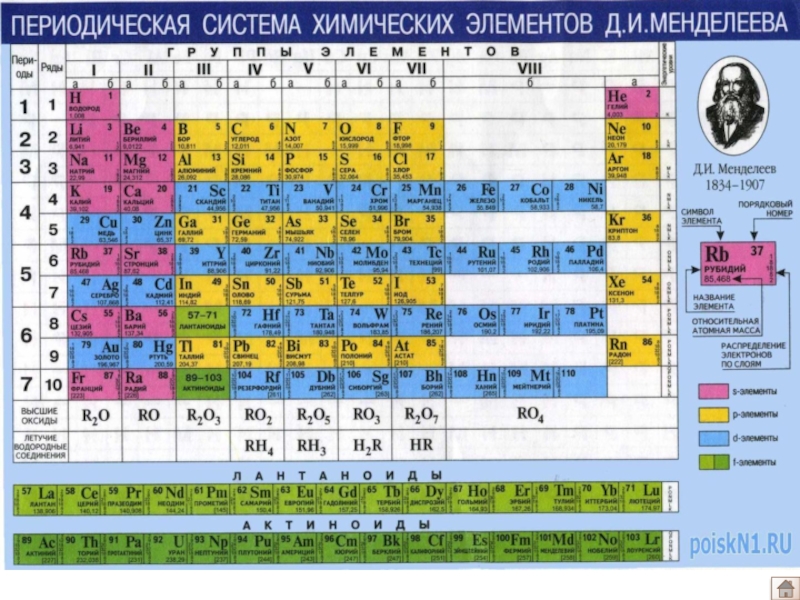
Таблица Менделеева
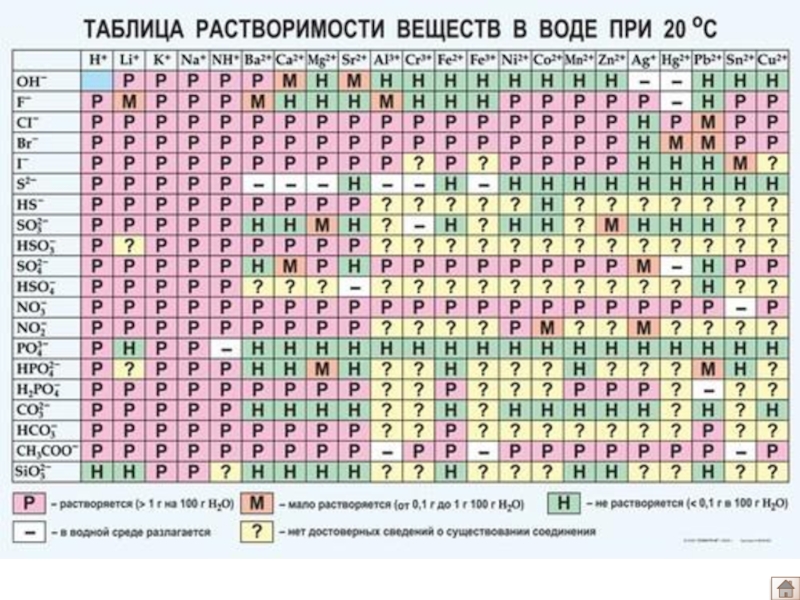
Таблица растворимости
Слайд 4Неверно
Неверно
Неверно
Верно
1) верны оба суждения
2) обы суждения неверны
4) верно
только А
3) верно только Б
25. Верны ли следующие суждения
о синтезе метанола и аммиака в промышленности? А. Реакции синтеза метанола и аммиака экзотермические. Б. В производстве метанола и аммиака применяется циркуляционный
ТМ
ТР
Слайд 5Верно
Неверно
Неверно
Неверно
4) 8,4 г
2) 4,2 г
1) 2,8 г
3) 5,6 г
26. Какую массу
оксида кальция необходимо взять для приготовления 200 г раствора гидроксида кальция с массовой долей 3,7%? ТМ
ТР
Слайд 6Верно
Неверно
Неверно
Неверно
4) 5,6 л
2) 22,4 л
1) 33,6 л
3)
11,2 л
27. В результате реакции, термохимическое уравнение которой
2С2Н2 +5О2
= 4СО2 + 2Н2О + 2610 кДж.Выделилось 652,5 кДж теплоты.
Объем сгоревшего ацетилена равен
ТМ
Слайд 7Неверно
Неверно
Неверно
Верно
1) 50
2) 40
4) 60
3) 30
28. Сколько литров
кислорода потребуется для каталитического окисления 100 л оксида серы (IV)
до оксида серы (VI)? Объёмы газов измерены при одинаковых условияхСлайд 8B1. Установите соответствие между названием вещества и классом (группой) неорганических
соединений, к которому оно принадлежит
классы соединений
1) алкен
2) одноатомный спирт
3) многоатомный
спирт4) простой эфир
5) сложный эфир
название вещества
А) CH3OCH3
Б) HOCH2CH2CH3
В) HCOOCH2CH3
Г) CH3C(OH)2CH3
Неверно
Верно
Неверно
Неверно
4) 4352
2) 1523
3) 4253
1) 2351
Слайд 9B2. Установите соответствие между названием вещества и степенью окисления углерода
вещества
степень окисления СА) метанол 1) –4
Б) метановая кислота 2) –3
В) метан 3) –2
Г) этан 4) 0
5) +2
6) +4
Неверно
Верно
Неверно
Неверно
4) 4352
2) 1523
1) 3512
3) 2351
ТМ
Слайд 10B3. Установите соответствие между веществом и продуктом на аноде при
электролизе его раствора
формула соли продукт на аноде
А) Na2CO3
1) H2SБ) Na2S 2) Cu
В) NaNO3 3) O2
Г) CuCl2 4) Cl2
5) S
6) CO2
Неверно
Верно
Неверно
Неверно
4) 1452
1) 1423
2) 3534
3) 3351
ТР
Слайд 11B4. Установите соответствие между формулой соли и её способностью к
гидролизу.
формула соли
1)Al2S3
2)K2SO3
3)CrCl3
4)K2SO4
Неверно
Верно
Неверно
Неверно
4) 1412
1) 1213
2) 3214
3) 3141
отношение к гидролизу
1)по катиону
2)по аниону
3)по катиону и аниону
4)гидролизу не подвергается
ТР
Слайд 12B5. Установите соответствие между реагентом и продуктом реакции
Реагенты
А) СО2
+ Н2О
Б) СО2 + СаО
В) СО2 + Са(ОН)2
Г) СО2(из6ыток) + Са(ОН)2
Неверно
Верно
Неверно
Неверно
4) 6123
1) 1213
2) 6234
3) 1241
Продукты
1) СаСО3
2) СаСО3 + Н2О
3) Са(НСО3)2
4) Са(НСО3)2+ Н2О
5) СО + Н2
6) Н2CO3
ТР
Слайд 13
B6. Установите соответствие между двумя веществами и реактивом, с
помощью которого можно различить эти вещества:
ТМ
Вещества
РеактивА) бутанон-2 и этанол 1) HCl (р-р)
Б)гексен-1 и этилформиат 2) FeCl3 (водн)
В)анилин и фенол 3) Br2 (водн.)
Г)бензол и анилин 4) Na
5) HNO3
Неверно
Верно
Неверно
Неверно
4) 4323
1) 4364
2) 2561
3) 1453
Слайд 14Неверно
Верно
Неверно
Неверно
4) 135
1) 236
2) 134
3) 145
B7. Как для бензола, так
и для стирола характерны
1) наличие в молекуле сопряженной электронной системы
2)
sp3-гибридизация атомов углерода3) взаимодействие с водородом в присутствии катализатора
4) обесцвечивание бромной воды
5) горючесть
6) хорошая растворимость в воде
Слайд 15Неверно
Верно
Неверно
Неверно
4) 456
1) 235
2) 156
3) 146
B8. Метанол вступает в реакции
с
CH3COOH
NaOH
Ag2O(NH3)
Br2(H2O)
KMnO4(H+)
Na
Слайд 16Неверно
Верно
Неверно
Неверно
4) 234
1) 136
2) 256
3) 145
B9. И анилин, и диметиламин
реагируют с
1) водой
2) бромэтаном
3) серной кислотой
4) бромоводородом
5) гидроксидом натрия
6) раствором
перманганата калияСлайд 17C1. Используя метод электронного баланса, составьте уравнение реакции:
NaNO2+NaI+...=NO+...+Na2SO4+...
Определите окислитель
и восстановитель.
Ответ: 2NaNO2+2NaI+2H2SO4=2NO+I2+2Na2SO4+2H2O
N+3 + e- -> N+2 окислитель
2I- + 2e-
-> I2 восстановительСлайд 18C2. Медь растворили в концентрированной серной кислоте. Полученную соль обработали
избытком раствора гидроксида натрия.
Выпавший голубой осадок отфильтровали и прокалили. Затем,
полученное вещество прокалили с углём.Напишите уравнения четырёх описанных реакций.
Ответ: 1) Сu+2H2SO4 конц. = CuSO4 + SO2 + 2H2O
2) CuSO4 + 2NaOH = Na2SO4 + Cu(OH)2
3) Cu(OH)2 = CuO + H2O
4) 2CuO + C = 2Cu + CO2
Слайд 19C3. Напишите уравнения реакций, с помощью которых можно осуществить
следующие превращения.
Al4C3 + 12H2O → 3CH4 + 4Al(OH)3
2CH4 → C2H2 +
3H23C2H2 →C6H6
C6H6 +Br2 → C6H5Br + HBr
C6H5Br + 3NH3 → C6H2Br(NH2)3 + 3H2
Х1 CH4 метан; Х2 CH4 ацетилен; Х3 C6H6 бензол;
Х4 C6H5Br бромбензол; X5 C6H2Br(NH2)3 1-бром-2,4,6-триаминбензол
(+H2O) 15000С Сакт. t0 (+Br2), AlBr3 (+NH3), t0, p
Al4C3 → Х1 → Х2 → Х 3 → Х4 → X5
Слайд 20C4. Сероводород, выделившийся при взаимодействии избытка концентрированной серной кислоты с
1,44 г магния, пропустили через 160 г 1,5%-ного раствора брома.
Определите массу выпавшего при этом осадка 1) 5H2SO4конц. + 4Mg = 4MgSO4 + H2S + 4H2O
Br2 + H2S = 2HBr + S
2) n(Mg ) = 1,44/ 24 = 0,06 (моль)
n(H2S)=0,015 (моль)
n(Br2) = 160⋅0,015/160=0,015 (моль) (оба вещества реагируют полностью)
3)n(H2S)=n(Br2)=n(S)=0,015 (моль)
m(S)=32г/моль 0,015 моль=0,48г
Ответ: масса осадка = 0,48 г.
Слайд 21C5. При взаимодействии 11,6 г предельного альдегида с избытком гидроксида
меди (II) при нагревании образовался осадок массой 28,8 г. Выведите
молекулярную формулу альдегида. 1) СnH2nO + Cu(OH)2 = СnH2n+1O2 + H2O + Cu2O
2) n(Cu2O) = 28,8/144= 0,2 (моль)
n(Cu2O) = n(СnH2nO) = 0,2 моль
М(СnH2nO) = 11,6/0,2 = 58 г/моль
3)М(СnH2nO) = 12n + 2n + 16 = 58
14n + 16 = 58
14n = 42
n = 3
Молекулярная формула – C3H6O - пропаналь
Слайд 24Литература:
1. Открытый банк заданий ЕГЭ http://www.fipi.ru/os11/xmodules/qprint/afrms.php?proj=
2. http://chem.reshuege.ru/test?theme=20
3. http://www.otbet.ru/ege/demo-varianty-ege/demo-himiya/
4. О.С. Габриелян.
Химия 10 класс. Дрофа. М. 2012
5. О.С. Габриелян. Химия 11
класс. Дрофа. М. 20126. Шаблон Алексеевой Л.А.